※記事に記載された所属、職名、学年、企業情報などは取材時のものです
世界中でさまざまな企業や大学が研究を続けているにも関わらず、未だその全容が明らかになっていない膜タンパク質。その構造を解明するため、精製から構造解析、阻害剤や結合抗体のスクリーニングなど、多岐に渡る技術開発を続けてきたのが千葉大学の村田武士教授である。村田教授の研究はさまざまな創薬の開発に大きく寄与しており、今後世界から注目される可能性が非常に高い。2021年にはアカデミア創薬を実現するべく「膜タンパク質研究センター」を設立、産官学の融合や国際連携を進めている。センターの設立によりさらなる活躍が期待される村田教授に、これまでの経緯と膜タンパクの役割を分かりやすく解説していただいた。

村田 武士 教授
膜タンパク質の役割とは〜タンパク質はあらゆる生物の根本
「タンパク質」と聞くと栄養素を思い浮かべる人が多いと思いますが、実は私たちの目が見えるのも、筋肉が動くのも、タンパク質の機能によるもので、生物の全てがタンパク質によって動いていると言っても過言ではありません。遺伝子はタンパク質の設計図であり、病気は遺伝子が変異しタンパク質に傷がつくことによって起こるケースが大半です。
タンパク質全ての約1/3を占めている膜タンパク質は細胞を構成する脂質膜の中に存在しており、ほとんどの病気と関係します。またヒトの体は侵入してきた異物に対して免疫を誘導しますが、この時最初に異物を認識したり、細胞間のやり取りをしたりするのも膜タンパク質です。このように膜タンパク質は重要な働きをすることから、多くの製薬企業はその形を考慮しながら薬をデザインしています。実際皆さんが飲んでいる薬のうち6割くらいは膜タンパク質に結合し、機能を変えるという仕組みで作られています。
世界中で研究されている膜タンパク質
ところが膜タンパク質の形を解明することは非常に難しく、今までほとんど解明されてきませんでした。長い医学の歴史の中で、初めてヒトの膜タンパク質の形が分かったのは2006年。その後、一つの形が明らかになると国際的な科学ジャーナル誌であるネイチャーに載るほどのインパクトで注目されています。現在も多くの研究者が研究を重ねていますが、まだ大部分が解明されていません。そこで私たちはどのようにすれば膜タンパク質の形を解明できるか、という基盤技術を長い間作っているのです。
1994年から現在まで続く村田教授の研究
(1)生物学の研究で見えてくる世界の多様性
私が研究室に入った1994年ごろの生物学は未解明なことばかりで「まだ明らかになっていないことを解明する」ということに魅力を感じました。生物学を勉強していると「人間とは何か」「なぜ行動するのか」など、根源的なことが見えてくる感覚があります。遺伝子が分かり、タンパク質が分かり、病気がなぜ起こるのかが分かってくる。遺伝子やバクテリアが進化を繰り返してあるものは人間に、あるものは植物になり、多様性が生まれる。生物現象は分かっていないことがとても多く、研究していくと新しいことが見える喜びがあるのです。
(2)ノーベル化学賞を受賞した博士のもとで構造解析を学ぶ
1997年にアメリカのポール・ボイヤー博士とイギリスのジョン・ウォーカー博士がアデノシン三リン酸合成酵素という膜タンパク質の立体構造の一部を解明し、ノーベル化学賞を受賞しました。膜タンパク質の構造解明はそこまでインパクトのあるできごとなのか、と思うと同時にこういった分野で研究をしたいと思いました。そこで私は2000年に学位を取ると、渡英してケンブリッジ大学のジョン・ウォーカーラボに入りました。イギリスにいる間にアデノシン三リン酸合成酵素の形が分かるよう壊さずに取り出す精製技術を開発し、ジョン・ウォーカー博士が明らかにしたものとは別の部分の精製と構造解析に成功。この研究は国際的な科学ジャーナル誌・サイエンスに発表することができました。
(3)理化学研究所経て、京大医学部で世界的に有名な膜タンパク質構造解析技術を磨く
2005年には日本に戻り、理化学研究所の「基礎科学特別研究員制度」に採択され、自分がやりたいテーマを自由に3年間研究しました。その後、世界的に有名な膜タンパク質構造解析の専門家である京都大学医学部の岩田想教授の下でヒト膜タンパク質構造解析の新しい技術開発を進めました。その後2009年に千葉大学に移って研究を続け、2012年には開発技術を用いてヒト膜タンパク質(アデノシン受容体)の構造を明らかにし、ネイチャー誌に発表することができました。
膜タンパク質研究センターの設立
(1)基盤技術の開発
千葉大学のラボも大きくなって研究の幅も広がり、これまで培った解析技術を別の膜タンパク質にも使えるように基盤技術という形で特許を出願しました。さらに産学連携のプロジェクトで製薬企業のお手伝いをしていくうち、次のステージに進みたいという思いが芽生えました。製薬企業と組めば市場が必要としているターゲットを知ることができますし、私たちの技術の検証もできるのですが、もっと主体的に社会に貢献していきたいと考え、2021年10月に「膜タンパク質研究センター」を設立しました。
(2)アカデミア創薬の実現に向けて
設立後、センターに基盤技術を集約し、アカデミア創薬を進めるために学内外の共同研究者や製薬企業に参入いただきます。国家プロジェクト予算を獲得し、自分たちで薬のタネを作り、それを製薬企業の共同研究でピカピカの新薬に磨いていくプロセスを目標にしています。
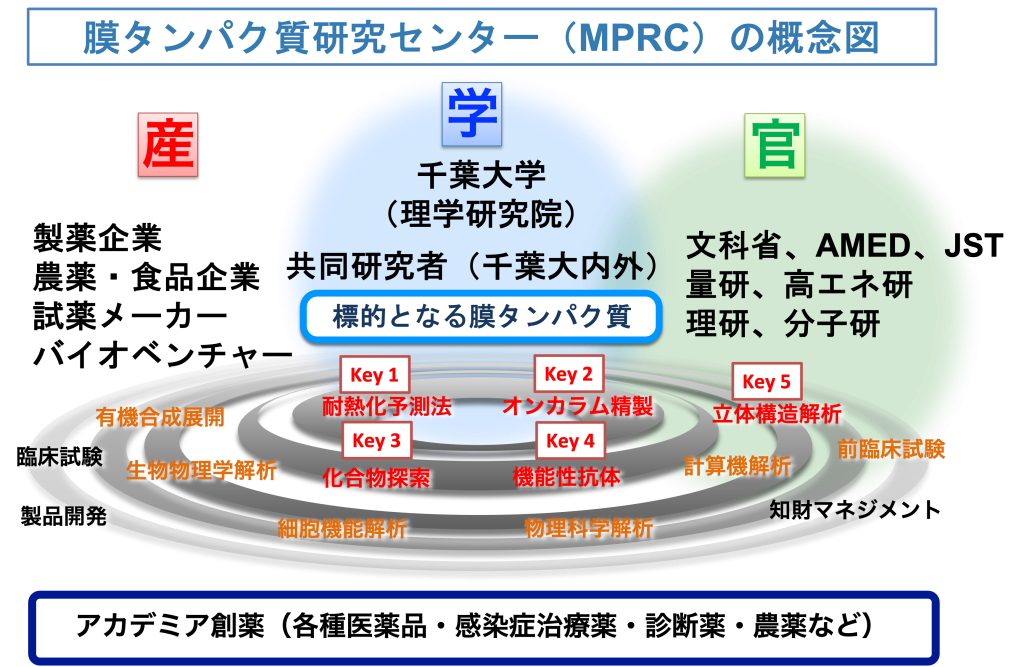
※膜タンパク研究センターがもつ革新的な5つの基盤技術(後述)
膜タンパク質構造解析に秘められたさまざまな可能性
耐熱化したタンパク質がもたらすメリットはまだたくさんあります。例えば光のエネルギーを変換し電気のエネルギーを作り出すロドプシンいうものがあります。我々は温泉の中に存在する菌から熱変性温度が92℃というロドプシンの耐熱性をさらに向上させ、世界で最も安定なロドプシン(熱変性温度115℃)を作り出すことに成功しました(プレスリリース)。煮沸しても壊れないので、いずれ出てくるであろうロボットの目や、センサーの材料として我々のロドプシンが役に立つかもしれません。また光のエネルギーを変換しているので光電池としても利用できる可能性もあります。そこで我々は世界で最も小さく効率のいい光電池を作るべく、東京工業大学と共同研究しています。
今後は人工細胞の素子としての使用や、膜タンパク質のエネルギー変換を応用して発電やクリーンエネルギーにも貢献していけるのではないかと考えています。このように創薬だけでなく、膜タンパク質にはさまざまな使い道があるのです。
世界に存在していないものを作り出す〜夢とチャンスが広がる膜タンパク質研究
こうした研究において、人材育成は非常に重要です。今、博士課程に進む学生が減少しているという現状があり、千葉大学でもいろいろなサポートをしています。ドクター資格は一度取得すれば一生ついてきますし、世界どこでも共通です。私もメール一つでジョン・ウォーカー博士のところに行くことができましたし、絶大な免許だと思います。私の研究室では所属学生に企業との共同研究やアカデミアの会合にも参加してもらっています。幅広い知識とオリジナルな研究分野を広げていく、そんな人材を育てていきたいと考えています。
膜タンパクの研究は、理論計算にしても薬にしても抗体にしても、世界中にまだ存在していない唯一のものを作り出して社会に貢献できる、夢のある研究だと思います。新型コロナウイルスを見ればわかるように、この研究によって世界を救うことができるかもしれない。そういったチャンスがあり、技術があるわけだから、夢を追いかけてほしい。もちろん難しいこともありますので、さらに技術開発をして成功率を上げていくように支援するのが研究室の役割だと考えています。
膜タンパク研究センターが持つ革新的な5つの基盤技術
Key1-1 独自の理論計算法による膜タンパク質の耐熱化変異体作製技術
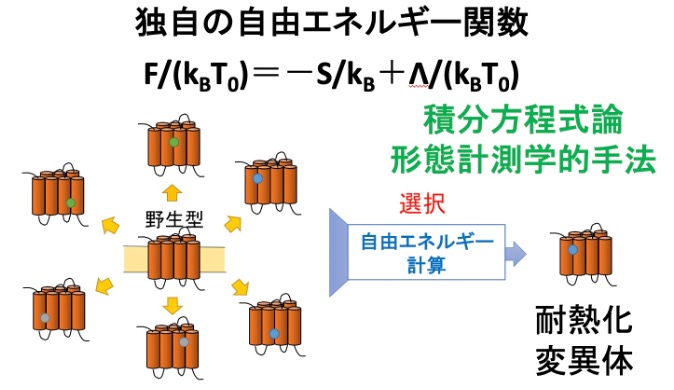
膜タンパク質精製の難しさはその耐熱性、熱安定性が弱いことにあります。実はヒトの組織として見た場合、膜タンパクは不安定な方が都合良く、一度働いたら分解するよう進化してきました。そのため人肌で壊れるほど脆いのです。けれど、20種類のアミノ酸が連なる一本の鎖が自発的に折り畳まれた特殊な形をしているタンパク質の形を明らかにするためには、まず膜タンパク質自体を安定になるように改変する必要があります。そこでアミノ酸の配列を、理論計算を使って壊れにくいものに変異させていくという「独自の理論計算法による耐熱化変異体予測技術」を理論計算の専門家である安田賢司特任助教、木下正弘招聘研究員(京都大学名誉教授)との共同研究で導き出しました。
PC上でアミノ酸の変異体を発生させて計算し、元の組み合わせより安定化する状態を選んでいきます。従来の計算機解析ではかなりの計算時間を要しますが、この計算方法では通常の1万分の1のスピードで計算できます。 この技術で国際特許も取り、製薬会社と共同研究も行っています。
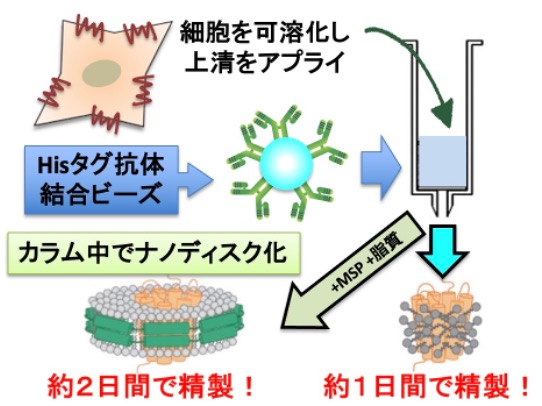
Key2 膜タンパク質の迅速精製技術
膜タンパク質の形や機能を理解するには、その膜タンパク質を綺麗に単離(精製)する必要があります。まず、細胞膜の膜タンパク質を界面活性剤(洗剤みたな物質)によって溶かし出し、わずか1日できれいに精製することができる独自の精製システムを開発しました。また、この精製システムでは、精製した膜タンパク質を再度膜の中に戻す、という「ナノディスク化」も可能です。現在、この迅速精製システムの特許を出願しています。
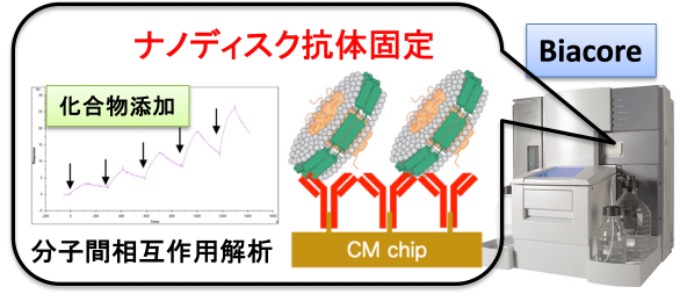
Key3 薬剤のタネとなる結合化合物スクリーニング技術
製薬企業はそれぞれ独自の化合物ライブラリを保有しており、その中から、標的タンパク質に結合できる化合物をスクリーニングします。これを効率的に行う技術が「結合化合物スクリーニング技術」です。我々は、独自のナノディスク抗体を作り出し、Biacoreと呼ばれる結合測定装置とこの抗体を用いることで、ナノディスク化した膜タンパク質に結合する化合物を効率的にスクリーニングする技術を開発。この技術を用いることで、簡便に薬のタネを見つけ出すことができるようになりました。
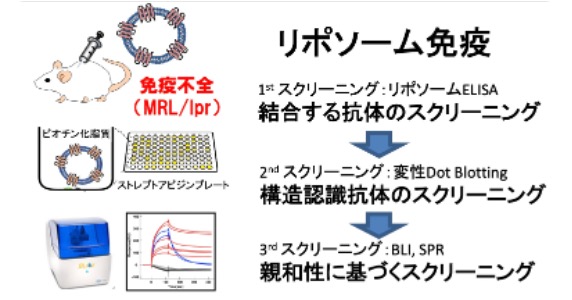
Key4 抗体医薬につながる機能性抗体の作製技術
最近の薬作りでは抗体が主流になりつつあります。世界で売れているTOP10の医薬品のうちの半分以上が抗体医薬品です。抗体医薬品とは、例えばがんでいえば、がん細胞だけに効く抗体を作り、それを体内に入れてがん細胞をピンポイントで攻撃する薬のことをいいます。先ほどの技術で精製した膜タンパク質をマウスに注入すると、マウスはこれに対する抗体を作ります。効果的な抗体を作るには、マウスに注入した膜タンパク質がなるべく長い時間、壊れない状態でいてくれることが重要であることを見出しました。これは先述の京都大学・岩田教授や小笠原諭特任准教授(元京都大学医学研究科研究員)との共同研究による大きな成果です。つまり、なるべく安定な膜タンパク質の変異体を作り出せるかが鍵になるわけです。このようにして、抗体医薬につながる効果的な抗体を作り出すことができるようになりました。
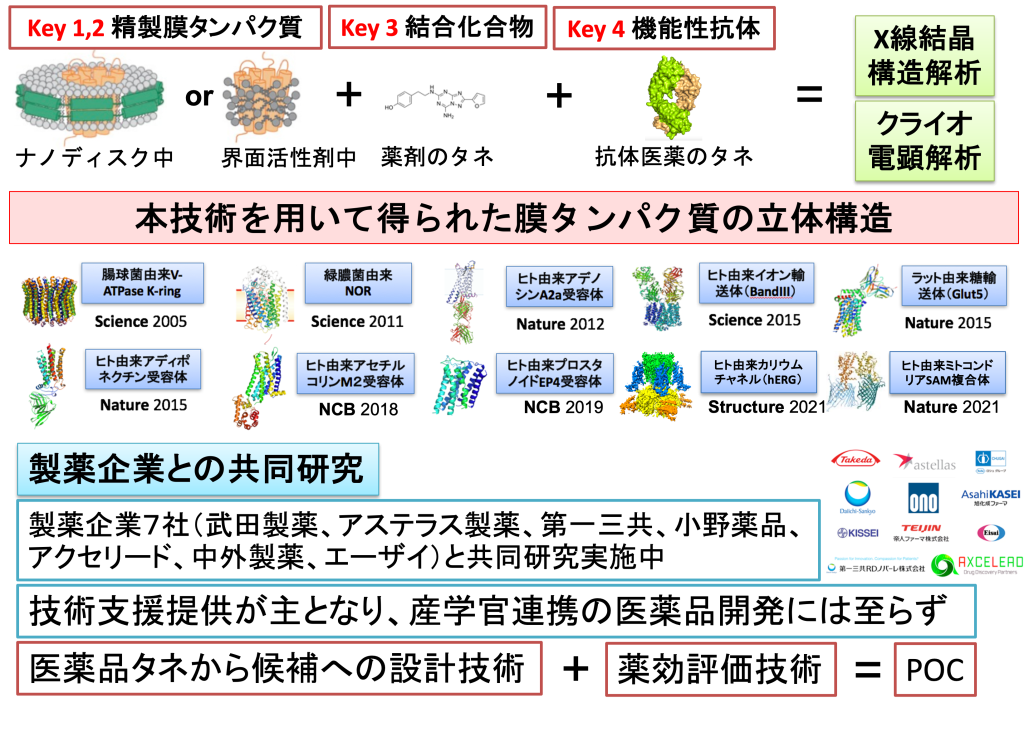
Key5 膜タンパク質の立体構造決定技術
タンパク質の詳細な形を明らかにする方法として、X線結晶構造解析とクライオ電子顕微鏡単粒子解析があります。どちらの方法でも目的のタンパク質の揺らぎや動きを固定してしまうことが重要であることが知られています。Key4で見つけた薬のタネを用いて膜タンパク質の動きを固定することができます。またKey5で作り出した抗体医薬のタネを用いて膜タンパク質の揺らぎを固定することができます。我々はこの2つの武器を用いて病気に関係する重要な膜タンパク質の詳細な形の情報を数多く得ることに成功しています。
連載
創薬からドローン・宇宙まで〜バイオ研究最前線
SDGsの達成とQOL向上に必要不可欠なバイオテクノロジーの推進。バイオテクノロジーとライフサイエンス分野のトップリーダーたちが挑むユニークな研究とは?

















